胶体中的化学
清晨,一缕晨光倾泻而下,在林间留下一条光亮的通路;卤水滴入豆浆,就能结成豆腐;黄河三角洲的形成,主要是含硅酸盐胶体的黄河水遇海水中的盐分发生了胶体的聚沉……这些现象都离不开胶体。胶体的性质多种多样,在生活中的应用也不胜枚举。
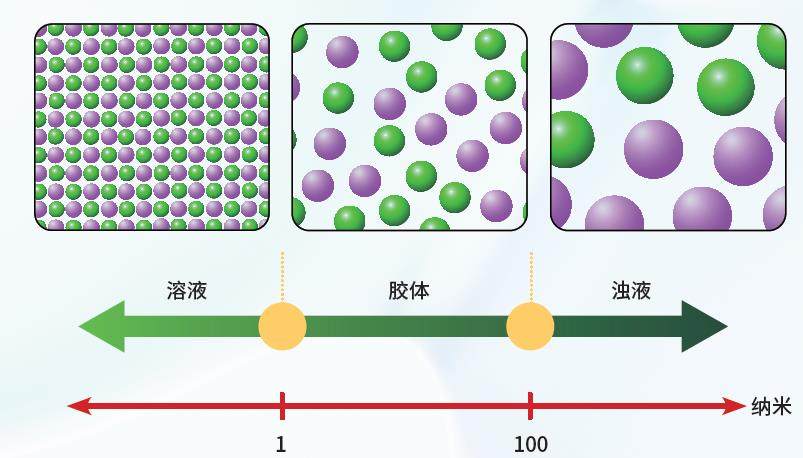
分散体系的划分
——什么是胶体?
在我们生活的环境中,多数物质是以两种或两种以上的純净物以混合物的形式存在。一种或者几种物质(分散相)分散到另一种物质(分散介质)中所形成的混合物体系,叫作分散体系,例如盐水溶液,其中氯化钠(NaCl)为分散相,水(H2O)为分散介质。
根据分散相粒径的不同,分散体系可分成3类:粗分散体系(浊液),例如含有泥沙的黄河水,泥沙能够通过肉眼观察到,该体系不能稳定地存在,静止后泥沙会沉淀,与液体分离;胶体分散体系;分子分散体系(溶液),例如盐水,氯化钠可以稳定地分散在水中,静置一段时间后,上层的口感与底层仍然一样,说明浓度一致。
胶体的分散介质可以是固体、液体和气体,根据其状态不同,可以将胶体分为固溶胶、液溶胶和气溶胶。

登录后获取阅读权限
去登录
本文刊登于《知识就是力量》2023年7期
龙源期刊网正版版权
更多文章来自

订阅





