近日,浙江大学刘智毅研究员、刘文杰博士合作课题组开发定量智能计算成像(ADQ)框架,该框架提供了一种生物医学显微成像的新范式,通过智能计算辅助传统光学显微镜帮助科学家找回数据中错失的信息。
自埃里克·白兹格等相关学者于2014年获得诺贝尔化学奖以来,超分辨显微成像技术近十年得到了蓬勃发展,大量新技术不断涌现,突破现有技术的成像分辨率、速度、深度等限制。但是每种技术均有其优缺点和适用范围,选择哪一种技术应对特定的问题是科学家们的困扰之一。
此外,超分辨显微成像技术的发展最终服务于相关生物应用,但是如何将技术发展和生物应用更紧密地结合,帮助生物学家更好地观察、发现和解释新现象,仍然是长期以来的难题。
面对上述问题,ADQ框架通过智能计算辅助传统光学显微镜充分挖掘潜藏的生物学信息,更好地助力生物学应用。
利用ADQ技术,研究人员研究了细胞骨架结构重塑与细胞迁移功能之间的关系,揭示了新现象。课题组发现了在单细胞迁移和多细胞互作诱导迁移这两种迁移方式中,细胞微管结构重塑的相似性和差异性。
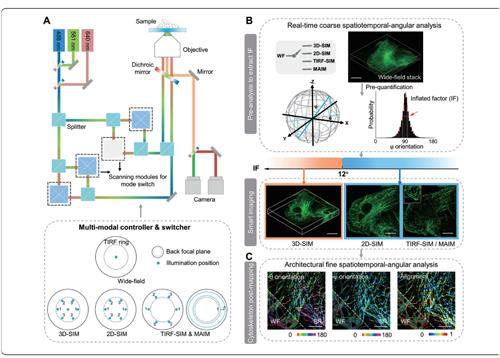
具体而言,在单细胞迁移中,微管在细胞迁移前端和尾端的空间重塑尤为剧烈;而在多细胞互作迁移中,微管在多细胞接触点附近运动活跃。
有趣的是,在这两种迁移方式中,微管呈现出一致的取向变化(DOC),并且与细胞迁移方向具有相关性。
这些微管结构重塑特征的发现,有助于研究者们更好地理解微管在细胞迁移过程中所发挥的力学功能,进而开展特异性细胞运动调控。
该研究应用前景广阔,为生物医学显微成像领域提供了一种新的研究范式。从技术创新角度而言,ADQ框架也可用于指导优化结构光照明显微镜(SIM)外的其他超分辨成像技术。
从生物应用角度来看,ADQ可用于研究纳米尺度下的多种亚细胞结构,如微管、微丝、内质网和线粒体等,有助于科学家更好地理解细胞迁移、代谢、凋亡等功能,进而启发个性化疾病调控、干预和治疗。
“该工作呈现得非常准确和详尽。该研究和方法同时为亚细胞动态和行为相关的基础和应用研究打开了新的大门。”
“该工作展示了超分辨显微成像技术和定量数据分析之间的协同力量和魅力,以及如何启发重要的细胞生物新发现。







